近年来,CAR-T细胞疗法在血液肿瘤领域取得了革命性突破,但复发/难治性B细胞非霍奇金淋巴瘤(R/R B-NHL)患者在接受CD19单靶点CAR-T治疗后仍有约半数会在约半年出现疾病进展,其中抗原逃逸是重要的耐药机制。如何进一步提高CAR-T治疗的深度与持久性,成为领域内持续探索的方向。

西比曼生物科技(AbelZeta)在今年三月底的2026年欧洲血液与骨髓移植学会(EBMT)年会上展示了其核心产品C-CAR039(CD20/CD19双靶点自体CAR-T产品C-CAR039,通用名:Prizloncabtagene autoleucel)治疗R/R B-NHL的长期随访数据。结果显示,中位随访53.9个月时,患者中位无进展生存期(PFS)达到60.1个月(5年),4年总生存(OS)率超过65%,且未出现新的安全性信号。这一长期数据将该双靶点CAR-T的临床获益推向了新的高度。
长随访验证持久疗效:半数以上患者实现5年无进展生存
C-CAR039是西比曼自主研发的一款靶向CD20和CD19的第二代自体CAR-T产品,采用4-1BB共刺激域。双靶点设计旨在克服肿瘤中CD20/CD19抗原表达的不均一性以及抗原丢失导致的复发。本次公布的是一项在中国4家中心开展的I期研究者发起的临床试验(IIT,NCT04317885等)的长期随访数据。
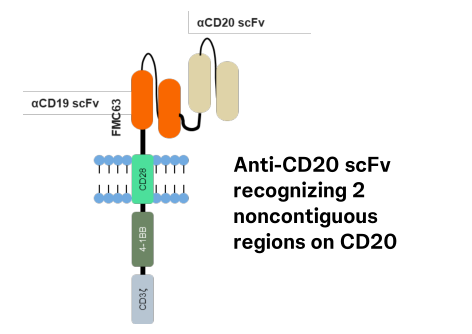
研究共入组48例R/R B-NHL患者,其中44例(91.7%)为预后较差的复发难治大B细胞淋巴瘤(LBCL)。这些患者中位既往治疗线数达3线,70.8%为难治性,75%处于Ann Arbor III/IV期,基线情况极为严峻。
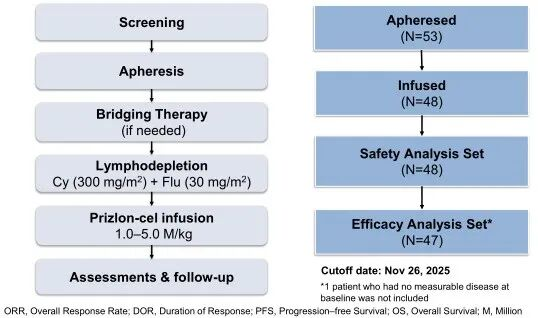
随着随访时间延长至中位53.9个月(范围3.1-72.2个月),C-CAR039展现出超乎预期的持久疗效。在全部48例患者中,客观缓解率(ORR)为91.5%,完全缓解率(CR)达85.1%;在LBCL亚组(43例)中,ORR和CR率分别为90.7%和86.0%。值得注意的是,许多初始仅为部分缓解(PR)的患者在后续随访中逐渐转化为CR,体现了双靶点CAR-T深度清除肿瘤的持续作用。
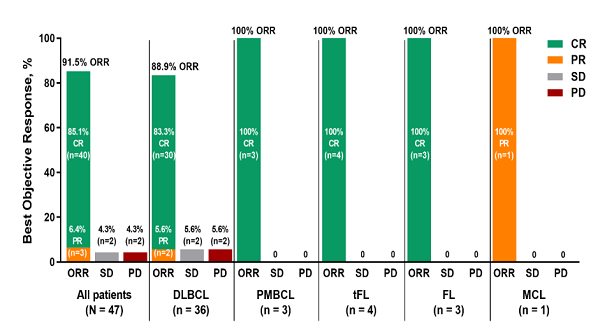
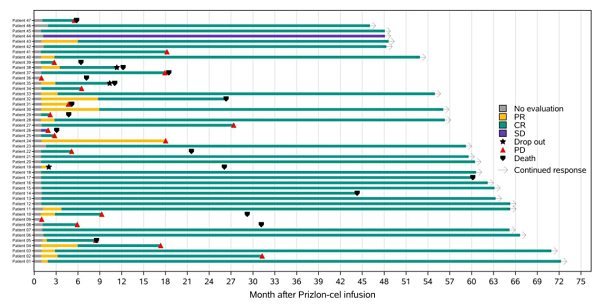
在长期生存获益方面,全部患者的中位PFS长达60.1个月(约5年),Kaplan-Meier估算的4年PFS率为53.3%;LBCL患者的4年PFS率同样达到54.2%。中位总生存期(OS)尚未达到,4年OS率在全部患者和LBCL患者中分别为65.9%和67.4%。这意味着,即使对于经过多线治疗失败的原发难治性淋巴瘤患者,C-CAR039也有望帮助超过半数实现4年以上无疾病进展生存,近七成患者存活超过4年。
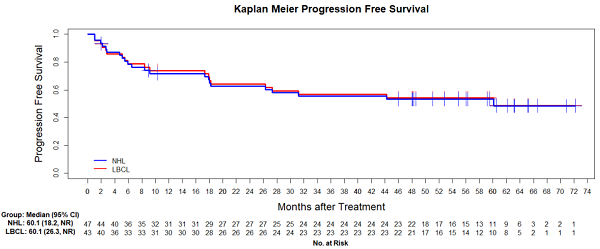
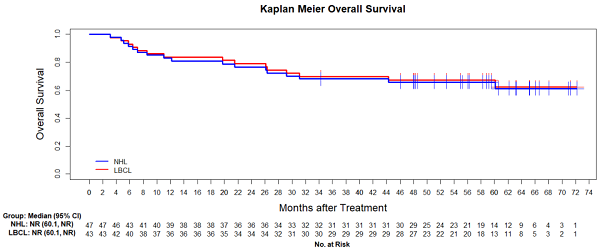
在LBCL患者中,28例(65.1%)在接近4.5年时仍存活,其中20例(46.5%)持续维持缓解且未接受任何后续抗淋巴瘤治疗,治疗后随访超过3年的患者均未发生疾病进展。这些数据有力证明了C-CAR039能够为患者带来长期、稳定且不依赖于额外治疗干预的疾病控制,展现出潜在的“治愈性”特征。
长期安全性稳定可控,临床管理要点明确
除疗效外,长期安全性是评估细胞疗法能否广泛应用的基石。本次更新数据显示,C-CAR039的安全谱与既往报道一致,未出现新的安全性信号。细胞因子释放综合征(CRS)总体发生率为93.8%,但≥3级严重CRS仅1例(2.1%);免疫效应细胞相关神经毒性综合征(ICANS)发生率为6.3%,且均为1-2级,未出现≥3级事件。这一低严重毒性特征与产品采用的4-1BB共刺激域设计以及双靶点可能带来的更均衡的T细胞激活有关。
长期随访中,最常见的≥3级不良事件仍为血细胞减少,其中中性粒细胞减少占83.3%,白细胞减少占50%。但大部分患者的血细胞减少在输注后90天内恢复,至第365天仅2例存在持续性的严重血细胞减少。临床需要关注的是,在输注后90天以上,仍有超过半数患者出现感染事件,其中带状疱疹感染率较高(18.8%)。
这提示CAR-T治疗后长期B细胞缺陷可能带来迟发性感染风险,建议在后续临床管理中加强对带状疱疹等感染的预防性抗病毒治疗。
临床进展显著提速,全球临床数据得到再次验证
自首例患者入组以来,C-CAR039已在中国完成了I期IIT研究的长期随访,并积累了53.9个月随访数据。基于这些扎实的临床证据,C-CAR039在国内的注册临床研究(NCT05800977)正在积极入组,针对复发/难治性大B细胞淋巴瘤(R/R LBCL)患者开展关键性试验。中国患者有望率先受益于这一具有国际竞争力的本土创新细胞疗法。
2023年,西比曼与强生公司(Johnson & Johnson)达成全球合作与许可协议,由强生负责C-CAR039(代号JNJ-90014496)在大中华区以外的全球开发。在2026年3月EBMT会议上,强生同步展示了JNJ-90014496全球1b(NCT05421663)期临床和转化医学研究结果。截至目前,强生已连续在2025年6月EHA、12月ASH和2026年3月EBMT会议上公布了全球1b期计量探索研究的初步数据,根据clinicaltrials.gov截至2026年4月的更新,该临床预计在超过30个全球临床中心预估入组超过400例患者。在强生全球1b期已公布数据的51例患者中,ORR达到91%,CR率为75%,疗效比已商业化的CD19单靶点CAR-T有明显优势。生物标志物分析同时显示,即使在CD20或CD19低表达、以及传统上被认为对CAR-T反应不佳的免疫抑制性肿瘤微环境(如TEX、FMAC亚型)中,C-CAR039仍保持了80%以上的高CR率。这些数据从全球多中心角度验证了双靶点的机制优势,也为后续注册奠定了基础。
双靶点CAR-T有望改写淋巴瘤长期治疗格局
对于复发/难治性大B细胞淋巴瘤患者而言,现有CD19单靶点CAR-T疗法的中位PFS通常在3-7个月之间,4年PFS率约30%-47%。C-CAR039此次公布的53.9个月随访数据——中位PFS达5年、4年PFS率超过53%——在目前所有CAR-T产品的长期数据中处于领先地位。尽管不同研究的患者基线存在差异,非头对头比较需谨慎,但双靶点策略在克服抗原逃逸、提升缓解深度方面的机制优势已获得临床数据的强力支持。
随着注册性研究的推进和长期随访的持续更新,C-CAR039有望成为复发/难治性B细胞淋巴瘤治疗的新标杆,再次印证CAR-T相比于其他modalities不可取代的独特优势,为全球患者带来真正的长期生存希望。
*本文数据来源:2026年EBMT大会壁报(中位随访53.9个月)、Blood杂志(2025;145:1526-1535)、EHA 2025及ASH 2025会议报告。*